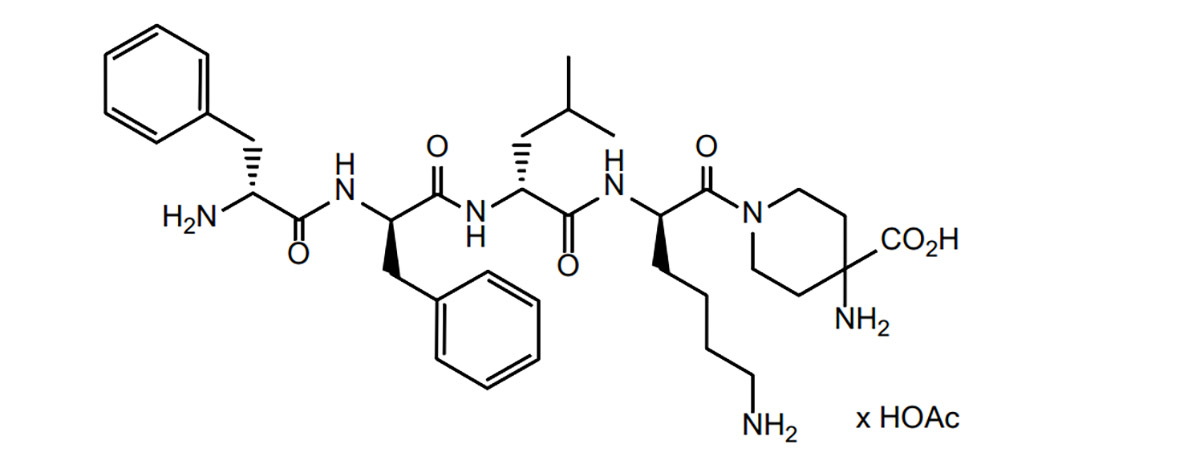
Уште на 24.08.2021 година, Cara Therapeutics и нејзиниот деловен партнер Vifor Pharma објавија дека нивниот прв агонист на капа опиоидните рецептори дифеликефалин (KORSUVA™) е одобрен од FDA за третман на пациенти со хронична бубрежна болест (CKD) (позитивен умерен/тежок пруритус со третман на хемодијализа), а се очекува да биде лансиран во првиот квартал од 2022 година. Cara и Vifor потпишаа ексклузивен договор за лиценца за комерцијализација на KORSUVA™ во Соединетите Американски Држави и се согласија да ја продадат KORSUVA™ на Fresenius Medical. Меѓу нив, Cara и Vifor имаат по 60% и 40% удел во профитот во приходите од продажба, освен Fresenius Medical; секој има по 50% удел во профитот во приходите од продажба од Fresenius Medical.
Пруритусот поврзан со ХББ (ХББ-aP) е генерализиран пруритус кој се јавува со висока фреквенција и интензитет кај пациенти со ХББ кои се на дијализа. Пруритусот се јавува кај околу 60%-70% од пациентите кои се на дијализа, од кои 30%-40% имаат умерен/тежок пруритус, што сериозно влијае на квалитетот на животот (на пр., лош квалитет на спиење) и е поврзан со депресија. Досега не постои ефикасен третман за пруритус поврзан со ХББ, а одобрувањето на Дифеликефалин помага да се одговори на огромниот јаз во медицинските потреби. Ова одобрување се базира на две клучни клинички испитувања од фаза III во поднесениот документ за независна медицинска помош: позитивни податоци од испитувањата KALM-1 и KALM-2 во САД и на глобално ниво, и дополнителни податоци од 32 дополнителни клинички студии, кои покажуваат дека KORSUVA™ добро се поднесува.
Неодамна, дојдоа добри вести од клиничката студија за дифеликефалин во Јапонија: 2022-10-1, Cara објави дека нејзините партнери Maruishi Pharma и Kissey Pharma потврдија дека инјекцијата дифеликефалин се користи во Јапонија за третман на пруритус кај пациенти на хемодијализа. Клинички испитувања од фаза III Примарната крајна цел беше исполнета. 178 пациенти примија 6 недели дифеликефалин или плацебо и учествуваа во 52-неделна отворена продолжена студија. Примарната крајна цел (промена во резултатот на нумеричката скала за пруритус) и секундарната крајна цел (промена во резултатот на чешање на скалата Ширатори) беа значително подобрени од почетната вредност во групата со дифеликефалин во споредба со плацебо групата и беа добро толерирани.
Дифеликефалинот е класа на опиоидни пептиди. Врз основа на ова, Институтот за истражување на пептиди ја проучил литературата за опиоидни пептиди и ги сумирал тешкотиите и стратегиите на опиоидните пептиди во развојот на лекови, како и моменталната состојба со развојот на лекови.
Време на објавување: 17 февруари 2022 година